Redacción Ciencia.- Un equipo científico ha creado una base de datos a gran escala con los cambios en el ADN que comparten humanos y otros mamíferos a lo largo de la historia, y que están relacionados con la duración de la vida, y ha desarrollado un «reloj biológico universal» capaz de estimar la edad de todos los mamíferos.
Se trata de una única fórmula matemática que calcula con precisión la edad de los tejidos de todas las especies de mamíferos, según los investigadores que, además, concluyen que la duración de la vida está estrechamente relacionada con las modificaciones químicas en el ADN.
Detrás de la investigación, que se publica en Science y en Nature Aging, está el Consorcio de Metilación de Mamíferos, una colaboración mundial que agrupa a casi 200 investigadores y que dirige Steve Horvath, experto en envejecimiento y profesor de la Universidad de California en el momento en el que se realizaron los estudios. Ahora investiga en los laboratorios Altos en San Diego.
«Hemos descubierto que la duración de la vida de los mamíferos está estrechamente relacionada con las modificaciones químicas de la molécula de ADN, lo que se conoce específicamente como epigenética o más exactamente metilación», describe Horvath.
La alimentación, el estrés o el tabaco pueden modificar la forma -no la secuencia- en la que se comportan los genes, lo que se conoce como epigenética. La metilación es un proceso que dirige cuándo y cómo son activados y desactivados los genes que controlan el normal desarrollo del organismo y que pueden verse afectados por causas ambientales.
Esta es esencial en el desarrollo y el envejecimiento de un organismo y, por lo tanto, desempeña un papel crucial en numerosas enfermedades y en la progresión de muchos cánceres.
Los dos estudios se centran en la metilación de la citosina, es decir, en la modificación química de esta; la citosina es uno de los cuatro componentes básicos de la molécula de ADN, recuerda un comunicado de la Universidad de California.
Los investigadores, entre los que también figura el español Juan Calor Izpisúa, científico fundador y director en los laboratorios Altos en San Diego, recogieron y analizaron datos de metilación de la citosina de más de 15.000 muestras de tejidos animales de 348 especies de mamíferos.
Un análisis exhaustivo, relata Horvath a EFE, que abarca prácticamente todos los tejidos imaginables: diversas regiones del cerebro, piel, riñón, hígado, pulmones, corazón, ovarios o bazo.
El equipo descubrió que las modificaciones en los perfiles de metilación son similares a los cambios en la genética a lo largo de la evolución, lo que demuestra que existe una evolución entrelazada del genoma y el epigenoma que influye en las características y rasgos biológicos de las diferentes especies de mamíferos.
La metilación, por tanto, tal y como se describe en Science, guarda una correlación sustancial con la duración máxima de la vida en todas las especies de mamíferos, y se observan diferencias entre las especies de más larga duración y las menos longevas.
Estas variaciones en los patrones de metilación indican probablemente diferencias en el desarrollo.
Los tejidos se examinaron con una plataforma diseñada y construida específicamente para este proyecto y en el análisis se usaron herramientas computacionales y estadísticas avanzadas.
En el estudio de Nature Aging se publican perfiles de metilación de un subconjunto de datos, de 185 especies de mamíferos.
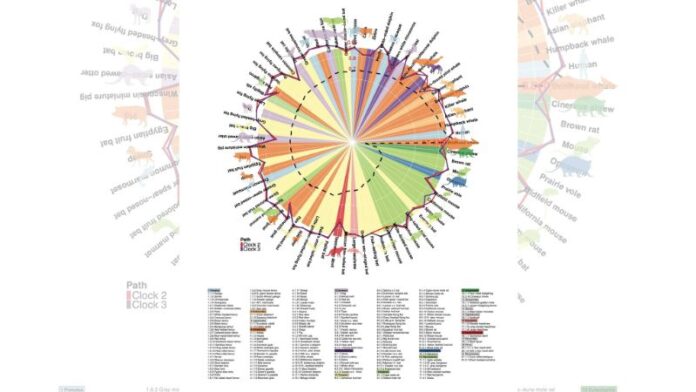
Se identificaron los cambios en los niveles de metilación que se producen con la edad y se desarrolló un «reloj panmamífero universal», una fórmula matemática que puede estimar con precisión la edad en todas las especies de mamíferos.
Horvath y un equipo de la Universidad de California introdujeron en 2011 el concepto de «reloj epigenético» para medir la edad, utilizando muestras de saliva humana.
Dos años después, demostraron que la metilación de la citosina permite crear un modelo matemático para estimar la edad en todos los tejidos humanos. El nuevo trabajo presenta una única fórmula que puede calcular con precisión la edad en todos los tejidos y especies de mamíferos.
«Gracias a nuestros descubrimientos, hemos dilucidado el papel continuo de la metilación en el envejecimiento», resume a EFE Horvath. «Aspiramos a que la comunidad investigadora aproveche nuestras herramientas -todos los datos están en abierto- para profundizar en los entresijos de la evolución de los mamíferos y la dinámica evolutiva del envejecimiento», agrega.
Izpisúa añade: «Estos estudios son pioneros para entender mejor el proceso de envejecimiento y nos ayudarán a trasladar a la clínica humana los descubrimientos que se están haciendo en distintos modelos animales». EFE